2026年3月10日
細胞膜修復の鍵を握るタンパク質を網羅的に同定
生命の進化において、細胞が内部環境と外部環境を隔てる能力を獲得したことは重要な転換点でした。細胞膜は、物質の出入りを制御し、細胞同士のコミュケーションや協調を可能にすることで、複雑な多細胞生物の基盤を支えています。
しかし、細胞膜は傷つきやすいものです。物理的なストレスや環境変化、細菌の毒素などによって細胞は頻繁に損傷を受け、修復が遅れると細胞は死に至ります。膜修復は細胞の生存に不可欠ですが、その詳細なメカニズムは長らく不明でした。その重要性は、膜修復に関わるタンパク質の変異がさまざまな疾患(筋ジストロフィー症など)を引き起こす事実からも明らかです。
このたび、沖縄科学技術大学院大学(OIST)の研究チームが、細胞膜修復の仕組みを新たに詳細に明らかにしました。出芽酵母をモデルに、膜修復に関わるタンパク質80種類(うち72種類は初めての同定)を特定し、その動きを蛍光顕微鏡によってリアルタイムで追跡しました。研究成果は科学誌『eLife』に掲載されています。本論文の筆頭著者で、OIST膜生物学ユニットに所属する山﨑裕太博士は、「これは細胞膜修復タンパク質初の大規模なデータセットであり、修復プロセスの全体像を理解するのに重要であると考えています」と述べています。
研究チームは、酵母GFPライブラリを用いたプロテオーム規模のスクリーニングと生細胞のタイムラプス観察(ライブセルイメージング)を組み合わせました。まず、数千の酵母タンパク質を、通常状態と細胞膜ストレス条件下で観察しました。次に、細胞膜ストレス条件下で局在が変化していたタンパク質を対象に、レーザーで単一細胞にごく小さな損傷を与え、その後のタンパク質の動きを時間経過とともに追跡しました。
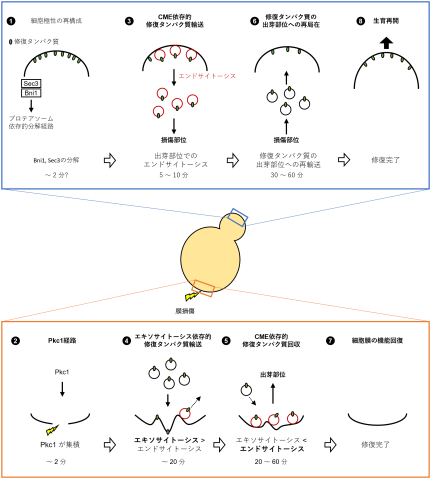
この結果、分子レベルでの協調的な一連のイベントが明らかになりました。最初に反応したのは、Pkc1シグナル伝達経路のタンパク質群です。次に起こったのはエキソサイトーシス(開口分泌)で、これは細胞内の小胞が細胞膜と融合して、傷口を塞ぐために不可欠な脂質や構造成分を供給するプロセスです。その後、クラスリン依存的エンドサイトーシス(CME)が続きます。これは細胞膜が内側にくぼみ、外部から脂質や膜タンパク質を取り込むためのポケットを形成するプロセスで、修復後の膜が正常な構造と機能を回復するのに役立つと考えられます。
Pkc1とエキソサイトーシスの関与は予想されていましたが、出芽酵母の修復過程でCMEが果たす役割は意外な発見でした。山﨑博士は「損傷部位でのエンドサイトーシスは哺乳類細胞では報告されていましたが、出芽酵母では確認されていませんでした」と説明します。「今回、酵母でも同様の現象が起こることを明らかにしました。これはエンドサイトーシスが、哺乳類と酵母が分化する以前から存在する古代の修復メカニズムである可能性を示唆しています。」
もう一つの重要な発見は、通常は成長中の出芽部位(新しい膜が作られる場所)に集まる多くのタンパク質が、通常の位置を離れ、損傷部位へ移動したことです。山﨑博士は「新しい膜を形成するタンパク質が、出芽部位での働きをやめて損傷修復に加わるのです」と述べています。「損傷修復の仕組みは、新しい膜形成の仕組みとよく似ているのかもしれません。」
山﨑博士は次のように結論付けています。「本データセットが、ヒト細胞を含む高等真核生物における細胞膜修復機構研究の基盤となることを期待しています。」研究グループは以前、細胞膜損傷と細胞の老化(さらには生物の老化)との関連性を発見しました。また、膜修復プロセスの欠陥が筋ジストロフィーなどの疾患と関係していることも知られています。こうした背景を踏まえると、細胞を基本単位とする生命に共通する古くからのメカニズムを解明する基礎研究は、将来の治療応用に向けた重要な一歩となるだけでなく、細胞の進化的起源や生命の根幹をなすメカニズムの解明にもつながります。
論文情報
報道関係のお問い合わせ