2026年3月31日
タンパク質の進化を制限する要因を解明
タンパク質は、理論上膨大な数が存在しうるにもかかわらず、現在知られているタンパク質の種類は、ほんのわずかにすぎません。それにもかかわらず、こうした限られた既知のタンパク質が、将来のタンパク質設計における主要な参考データとして利用されています。そこで、既に知られているタンパク質が本来あり得る多様性をどれだけ代表しているのかを理解することは、医療や生体触媒、バイオ材料の開発など、幅広い応用分野の戦略づくりに役立ちます。
科学誌『PNAS』に掲載された本研究では、沖縄科学技術大学院大学(OIST)、オーストリア科学技術研究所(ISTA)、ウィーン大学、そしてスペインの宇宙生物学研究センター(CAB)からなる国際研究チームが、タンパク質の進化と配列空間との関係を調べ、タンパク質の多様化を制限する要因を特定しました。この発見は、祖先タンパク質の形成を推進した要因として、DNAの組換えが重要であるという理論を裏づけるとともに、AIによる最先端のタンパク質設計手法の多くが抱える限界も浮き彫りにしています。
「現代のAI手法はタンパク質の設計に革命をもたらしていると考えられており、2024年のノーベル化学賞はAlphaFoldの開発チームに授与されました。しかし、こうしたAI設計手法の多くは、既知のタンパク質データベースを基に学習されています。既知のタンパク質が配列空間をどの程度代表しているかを理解しないまま、これらの手法が本当に多様なタンパク質を設計できると、どれほど確信を持てるでしょうか?」と、OIST進化・合成生物学ユニットを率いるヒョードル・コンドラショヴ教授は述べています。
タンパク質の世界を見渡す
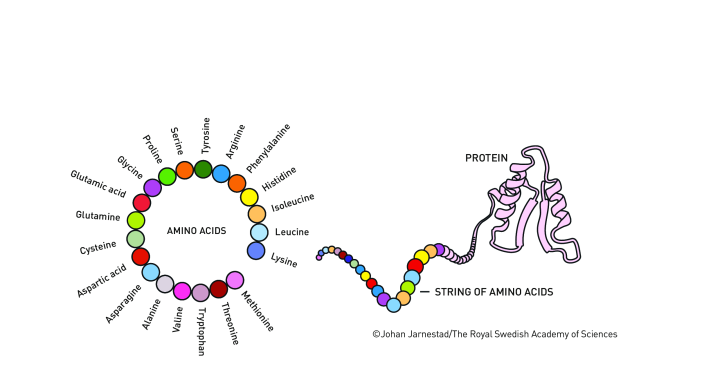
例えば、約20種類の異なるブロックを、さまざまな順序や割合で、何十個、何百個、さらには何千個もつないで鎖を作ることを想像してみてください。そのすべての組み合わせを描き出したものが「配列空間」と呼ばれるものです。
タンパク質の場合、その構成要素であるアミノ酸の形状や構造の制約により、考えうる配列のうち、正しい3次元構造に折りたたまれて生物学的機能を発揮することができる配列はごくわずかしかありません。タンパク質が3次元構造を保ったり、他の分子と結合したりするために必要な相互作用を生み出すためには、正しい化学基が正しい位置に配置されている必要があります。こうした要件を満たす配列だけを取り出していくと、実際に機能する配列空間はさらに狭まっていきます。
これらの機能的な配列のうち、進化の歴史の中で実際に存在したものは、比較的少ないと考えられます。そこで研究チームは、この限られたタンパク質が、機能空間をどの程度代表しているのかを明らかにしようとしました。
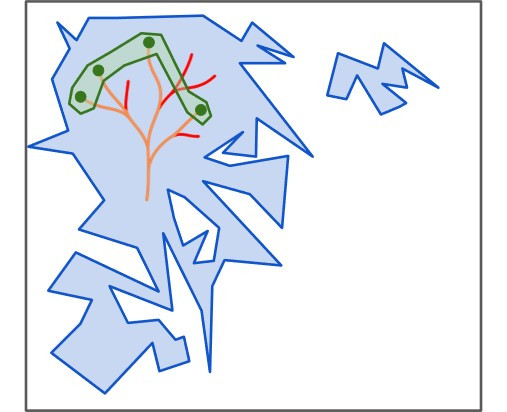
研究チームはまず、既知のタンパク質が占めている配列空間を数学的に記述することから始めました。次に、自然界に存在する多様なタンパク質ファミリーの構造がどのように多様化するのかを左右する生物学的要因を理解するために、タンパク質進化のモデルを構築しました。そして、そのモデルに基づいて、特定の生物学的機能に対して、どれだけの数の機能的な配列が存在し得るのかを予測しました。
既知のタンパク質の多様性を、こうしたタンパク質進化の理論的予測と比較した結果、研究チームは、進化の「出発点」が他の主要な進化プロセスよりもはるかに強く影響していることを発見しました。
「その出発点が主要な進化的制約になること自体は、必ずしも驚くべきことではありません。しかし、その重要性の大きさには本当に驚かされました」と、同ユニットの博士課程学生であり、筆頭著者であるラダ・イサコバさんは述べています。「進化生物学者として、今回の結果では自然選択やエピスタシスがほとんど影響していないように見えたことに興味をそそられました。」
タンパク質の進化を制限するものは何か?
特定のタンパク質をコードする遺伝子に変異が起こると、合成されるアミノ酸配列が変化し、それがタンパク質の進化につながります。自然選択によって、その変異がタンパク質の機能や安定性を高めるのか、あるいは損なうのかに応じて、どの変異が世代を超えて残るかが決まります。エピスタシス(異なる結果をもたらす遺伝的相互作用)も進化を制限します。個々の変異は単独では小さな影響しか持たなくても、別の変異と組み合わさると大きな影響を及ぼすことがあるためです。
自然選択とエピスタシスの両方がタンパク質の進化に影響を与えることは知られています。しかし、イサコバさんらの研究から、これらをはるかに上回ってタンパク質の多様性を制限している要因は「タンパク質の起源」にあることが明らかになりました。つまり、祖先タンパク質が存在していた配列空間の領域からの分岐は比較的小さいのです。
本研究は生命の起源に関する新たな知見を提供し、初期のタンパク質形成に関する既存の理論を裏付けるものです。イサコバさんは次のように説明しています。「私たちのシミュレーションでは、最後の普遍的共通祖先において最初のタンパク質が生まれたとき、利用可能だった時間的な制約を考えると、それらが単一の最初の配列の変異から単に分岐しただけでは説明がつきません。その代わりに、DNAの小さな断片がシャッフルされ、再結合することで、全く異なるタンパク質をコードできる新しいDNA分子が生み出されたと考えられます。」
また、研究チームは、本研究が実験科学者たちに新たな刺激を与え、既知の配列空間をさらに広げるきっかけになることを期待しています。イサコバさんは次のように述べています。「機能的なタンパク質を予測するニューラルネットワークの手法は、提供されるデータセットによって制限されています。そのため、既存のデータに基づく場合、ほとんどの手法は現在知られている配列空間を大きく超えて一般化することはできないでしょう。配列空間にはまだ広大な未踏領域が残っていますが、こうした未知の領域を切り開くには、新たな実験データが不可欠です。」
本国際共同研究の一部は科学技術振興機構(JST)の「先端国際共同研究推進事業(ASPIRE)」の支援を受けて実施しました。この助成金は、日本および世界のトップ科学者層のネットワークを構築し、将来持続的に世界で活躍できる人材を育成することを目的としています。
論文情報
報道関係のお問い合わせ