ナノ材料の細胞内輸送を効率化するらせん渦
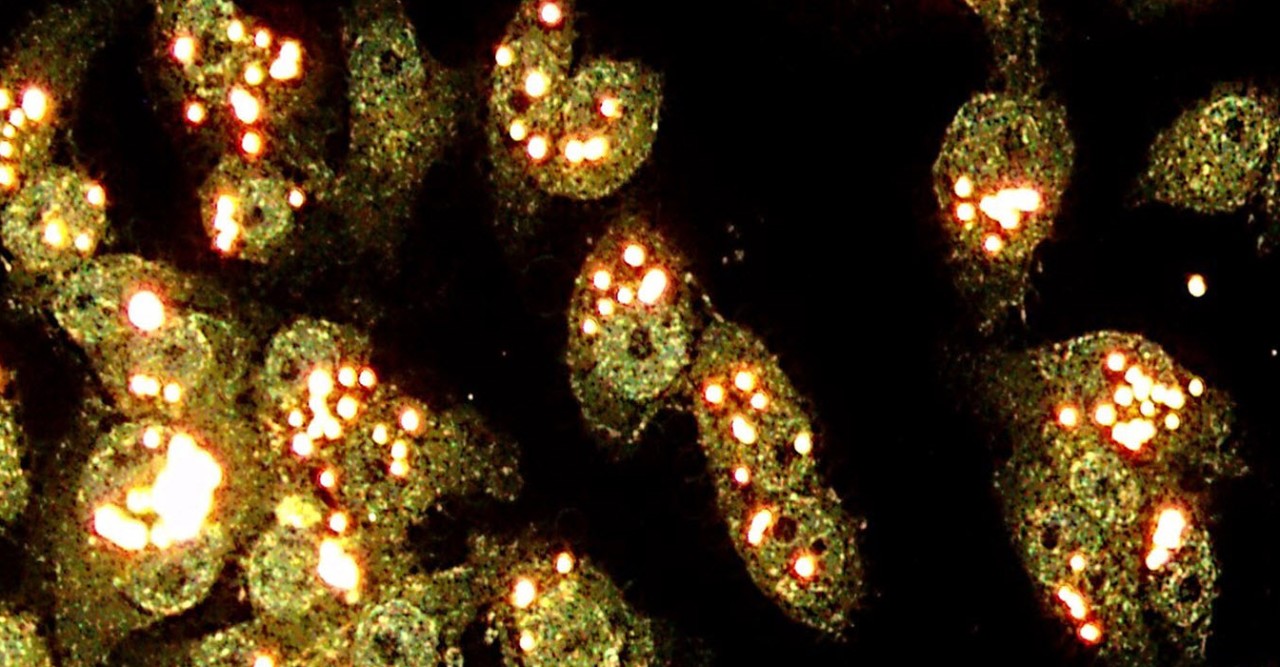
細胞を取り囲む細胞膜は選択的障壁として働き、細胞の内容物を包み囲むことで外部環境から保護し、細胞に出入りできる物質を選択する役割を担っています。しかし細胞膜のこの特性が、DNA、タンパク質、薬物などのナノ材料を細胞内に効率よく輸送する技術の開発を阻んできました。
この度、高麗大学校と沖縄科学技術大学院大学(OIST)の研究者らが共同で、細胞膜を変形させる微小ならせん渦を利用した、迅速かつ効率的な材料の輸送法を開発しました。本研究結果はACS Nano誌に掲載されました。
研究を率いた高麗大学校医療院のアラム・チョン准教授は、次のように説明します。「従来の細胞内輸送法には、スケーラビリティ、コスト、低効率および細胞毒性などの多くの課題がありました。本研究の目的は、これらの課題を解決する斬新な手法として、マイクロ流体力学で扱う,微小な空間での水の流れのふるまいを利用することでした。」
新たに開発されたマイクロ流体チップは「スパイラル・ハイドロポレーター」 と名付けられました。このチップ内では、毎分約100万個の細胞にナノ材料を96%の効率で輸送することが可能です。さらに、全工程を通じて細胞に不可逆的損傷を与えることがなく、最大94%の細胞が生き延びるのです。

「新たに開発したチップは手頃な価格で使用方法も簡単です。細胞とナノ材料を含む液体を両端に注入すると、ナノ材料を含んだ細胞が2か所の端からそれぞれ出てきます。プロセス全体にかかる時間はわずか1分です。」とチョン准教授は説明します。
流れに乗って
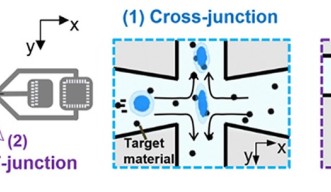
このデバイスは、マイクロ流体チップ内の流路の中央に十字交差部、上下に1つずつT字分岐部を持つように設計されました。
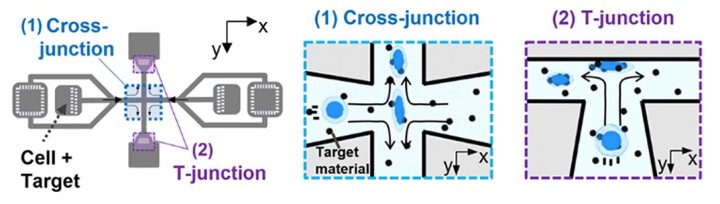
高麗大学校の研究者たちが、流路の形状や流速の違いが細胞にどのような影響を与えるかを調べ始めたとき、中程度の速さで流れる二つの液体が互いに反対方向から流れてきて衝突する十字交差内の特異なシナリオが目を引きました。
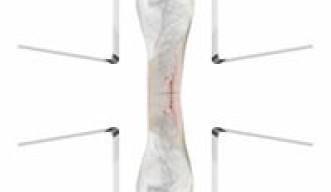
「細胞が十字型流路の中央で踊るように動き回るという非常に面白い挙動が観測されたのです。」とチョン准教授は話します。
そこで、液体の1つを蛍光色素で着色したところ、らせん形の渦が形成されていることを発見しました。
チョン准教授はまた次のように説明しています。「この現象を引き起こす流体力学を十分に理解したいと考えていたところ、OISTのエイミー・シェン教授が主宰するマイクロ・バイオ・ナノ流体ユニットが、この問題にすでに取り組んでいることを知りました。」
そこで2つの研究グループはチームを組みました。OISTの研究グループは学内のスーパーコンピュータを使用して、異なる流速で十字交差部で衝突する流体の流れがどのように相互作用するかをシミュレーションしました。
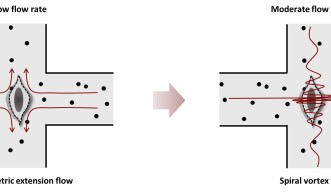
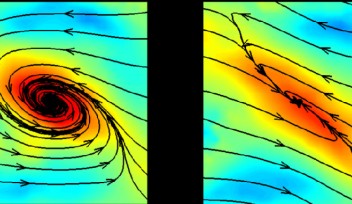
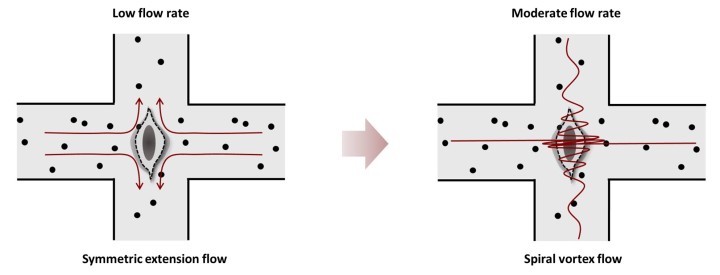
OISTのサイモン・ハワード博士は次のように説明しています。「研究論文の通り、低流速では衝突する2つの液体の流れが対称的に分かれ、十字交差部から流れ出ることがわかりました。しかし、流速を増加させると不安定性が生じ、複数の渦が形成されて、最終的に1つの大きならせん渦になることがわかったのです。」
「我々が開発したシミュレーションは、チョン准教授のグループが観測した異常現象を説明し、流速などの特定のパラメータがどのように渦形成に影響するかを正確に示しました。」とOISTのポストドクトラルスカラーであるダニエル・カールソン博士は付け加えました。
らせん渦の形成は、ナノ材料の細胞内への迅速かつ効果的な輸送の鍵となります。各細胞が十字交差部の中心を通過するとき、らせん渦の力が細胞を変形させ、膜に複数の微細なナノホールが生じます。流体中のナノ材料は、これらのナノホールから細胞内に入ることが可能になります。その後、細胞は十字交差部から押し流され、T字分岐部の壁に衝突し、細胞膜のさらなる変形を引き起こすことで輸送の効率を高めます。変形後、膜のナノホールは再び閉じられ、細胞膜は修復されます。
細胞生物学研究を促進
高麗大学校の研究チームはスパイラル・ハイドロポレーションを用いて、RNAや金ナノ粒子などの特定のナノ材料を細胞内に輸送することに成功しました。
DNA、RNA、CRISPR-Cas9などのタンパク質をより効率的かつ低コストで数多くの細胞に輸送することは、遺伝子治療、がん免疫療法、幹細胞などの研究に役立つ可能性があるとチョン准教授は話します。
金ナノ粒子は、薬物輸送、細胞内の分子や細胞小器官のイメージング、病気の診断にも活用することができます。
チョン准教授は次のように話しています。「スパイラル・ハイドロポレーションの応用は多岐にわたるため、高い関心を集めています。研究者たちは、より効率的で、シンプル、迅速かつ低コストの細胞内輸送手段を必要としています。私たちが開発したチップはそれを可能にする素晴らしい新技術なのです。」
広報・取材に関するお問い合わせ
報道関係者専用問い合わせフォーム