2017年4月24日
マイクロスケールにおける高分子溶液の流動挙動を解明
将来の医療分野にとって重要なコンセプトとなるのが、「ラボ・オン・チップ(LOC)」と呼ばれる装置の開発です。「チップ」と言っても、LOCはコンピュータに内蔵されている電子チップのことではなく、血液や尿など体液を流し込む特殊なマイクロスケールの流路(マイクロ流路)が加工された小さな装置のことを指します。このマイクロ流路に取り付けられたバイオセンサーにより、例えば、さまざまな疾患の可能性を示す体液中のバイオマーカーを検知し、素早い診断につなげることができます。
さらに、数センチ四方の装置にマイクロ流路を並べることで、一度にたくさんの検査が可能となります。しかしながら、1リットルの10億分の1にわたる極めて微量な量を流すため、新たな課題が生じます。観測手段の欠如から、このような微量な流体、特に生物由来の複雑流体が、マイクロ流路中でどのように振舞うかについて未だ十分な理解が得られていません。
OISTマイクロ・バイオ・ナノ流体ユニットのエイミー・シェン教授らは、マイクロ流体力学を駆使し、微小スケールでの複雑流体の振る舞いを制御する原理原則の解明に取り組んできました。今後は第二ステップとして、この研究から得られた成果を医療およびバイオテクノロジー分野での応用へと直接つなげていくことを目指します。同研究チームによる最新の研究成果は、米国物理学協会が発行する学術誌Journal of Rheologyに掲載されました。
マイクロスケールにおける高分子溶液の粘弾性特性を解析
高分子(ポリマー)は、いくつもの単量体分子(モノマー)が繰り返し結合した巨大な分子で、衣類やゴム、ポリスチレンといった私たちの身のまわりにある多くの合成素材を構成している物質です。高分子を液体に溶かした高分子溶液は、家庭用洗剤からペンキなど多くの市販品にも含まれます。一方、このような高分子溶液をマイクロスケールで用いると、医療診断ツールの性能を飛躍的に向上できる可能性があります。
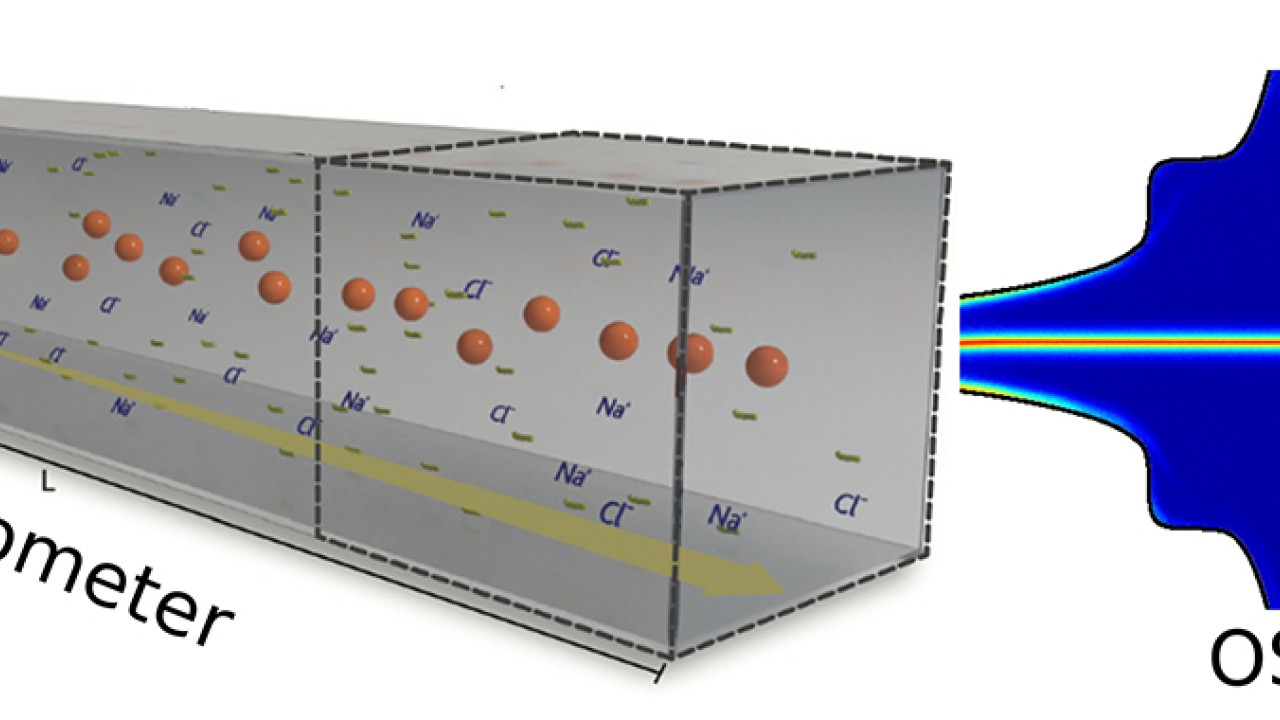
「水中に粒子を分散させた懸濁液に高分子を加えると、マイクロ流路中で新しい現象を引き起こします」、と同研究ユニットのフランチェスコ・デル・ジュディチェ博士は説明します。「これら高分子はバネのように振る舞い、懸濁液中の粒子あるいは細胞を一定方向に押しやり、流路内中央に整列させます」。マイクロ流路内で粒子や細胞を配列させることができれば、医療診断に用いるバイオセンサーのより効果的な使用に繋がります。また、細胞や大きさの異なる集合体から構成される血液などの生体液中の成分を、構成分子のサイズごとにふるい分けるといった作業が、高分子溶液を使うことで、全て一つのマイクロ流路チップ上で行える可能性もあります。
しかしながら、このような現象は高分子の性質に強く依存します。溶液中において、流れにより変形した高分子がもとの形状に戻るまでには一定の時間を要します。初期状態に戻るまでの時間を緩和時間と呼び、緩和時間は高分子の流動特性を特徴づけるための非常に重要なパラメータとなります。緩和時間は、市販の装置を用いることで見積もることができます。しかしながら、現在の技術では市販の装置を用いて測定できる緩和時間の範囲は限られており、高分子の濃度が低い希薄溶液、つまり、緩和時間が短い場合、多量の測定溶液が必要であったり、その緩和時間を定量的に見積もることは困難となります。
今回の研究では、デル・ジュディチェ博士と同チームのサイモン・ハワード博士が新たにマイクロ流体デバイスを設計し、内径マイクロメートルの流路を流れる高分子の変形と緩和時間を測定しました。この装置を使えば、少量および低濃度の高分子溶液の場合でも、溶液中の高分子に伸長やせん断変形を自由に与えられ、それら変形に対する応答を観測することができます。結果として、これまで測定できなかった、非常に短い緩和時間を示す希薄溶液であっても、その流動特性を明らかにすることができ、マイクロ流体デバイスを用いることで、高分子希薄溶液の流動特性のさらなる理解へと繋がると期待されます。
新たに作製したマイクロ流体ツールを使って、既に緩和時間が分かっている多種多様な高分子溶液のカタログを作成することもできます。このようなデータベースが実現すれば、チップを使って調べたい生体液における分子の整列および分離に最適な高分子を研究者が自由に選択できるようになります。「高分子溶液の性質が分かれば、一つのチップ上に複数の異なるモジュールを付け加え、いくつかの分析を同時に行うことが可能な高処理能力を備えたプラットフォームが実現します」と、デル・ジュディチェ博士は期待をにじませます。
報道関係のお問い合わせ