2016年12月22日
マイクロ流体装置で革新するセンサー技術
近年、マイクロ流体プラットフォームと呼ばれる技術によって、医療診断は革命的な進歩を遂げています。例えば、血液や尿サンプルを専門の分析機関に送ることが不要となり、医者は患者からの一滴の血液や尿サンプルから様々な疾患を診断することが可能となってきました。これらの診断技術は高価な機器は不要で、簡便で迅速な診断法「ポイント・オブ・ケア(Point Of Care:POC)」と呼ばれています。
これらの診断技術では、検査サンプルを測定する前に疾患を検出するため生体分子試薬(タンパク質やDNA等)をマイクロ流体プラットフォームの中に注入する操作を伴いますが、この操作では検査サンプルに押し流されないように生体分子試薬を装置の中にしっかりと固定することが求められ、操作にも時間を要します。そのため、マイクロ流体プラットフォームにあらかじめ生体分子試薬を内部に固定することができれば、迅速な診断に役立つことが期待できます。
しかしながら、マイクロ流体プラットフォームの装置を組み立てる際に、高エネルギーのイオン化ガスの照射を伴う密閉処理が必要が必要であるため、あらかじめ生体分子試薬を装置の中に固定した場合には、イオン化ガスの処理によって試薬がダメージを受けることが懸念されますが、一体どの程度のダメージを生体分子が受けるのか、よく分かっていません。
この謎を解明するため、沖縄科学技術大学院大学(OIST)の研究チームは従来のセンサーよりも正確に生体分子を検出することができる新しいセンサーを開発しました。同チームは、このセンサーを使用し、マイクロ流体デバイス内に生体分子を無事に固定できることを検証しました。
英国王立化学会(The Royal Society of Chemistry)が刊行する学術誌 Nanoscale に掲載された本研究成果は、より簡便な血液検査や尿検査を可能とするマイクロ流体プラットフォームの創出を加速させ、医療診断技術への大きな波及効果を生み出すと期待されます。
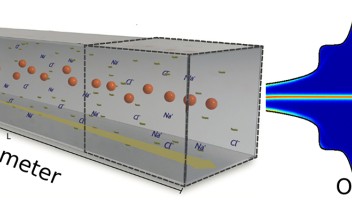
これまで、基板表面上での生体分子の有無を検出する技術として、センサー表面の微小な電荷の変化を検出可能な金属酸化半導体(Metal Oxide Semiconductor: MOS)を利用したセンサーが開発されてきました。このセンサーは、シリコン、半導体層、ガラス絶縁層、そして金薄膜から構成され、信号を検出するための電気回路に接続して使用します。そして,センサーの上面に電解質溶液で満たされたプラスチック容器を配置し、あらかじめ生体分子はセンサー表面に定着しています。このセンサーに電圧を加えて電流を計測すると、静電容量(キャパシタンス)の変化から電荷を算出することができます。この原理を応用すると、異なる電荷を持つ生体分子に由来する静電容量の変化を検出でき、生体分子の有無を定量化することができます。
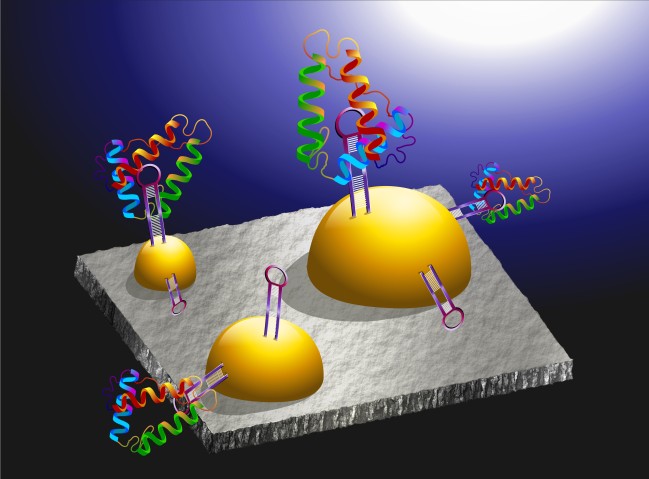
OISTマイクロ・バイオ・ナノ流体ユニットの研究チームが開発したセンサーは、従来のセンサーと同様の技術を使っていますが、生体分子の質量を検出する新たな機能を有しています。従来の金薄膜層を用いない本センサーは、ナノ金属絶縁半導体(nano Metal Insulator Semiconducter: nMIS)と呼ばれるタイプで、金薄膜を微小な島状に配置した構造となっています。このナノスケールの構造に光を照射すると、金表面の電子が特定の周波数で振動を始めます。そこに生体分子をセンサー表面に添加すると、生体分子の質量に応じて、その周波数が変化します。この変化を利用すれば、生体分子の質量を算出できことから、マイクロ流体プラットフォームを密閉する工程で生じる生体分子に対するイオン化ガス暴露の影響を検証することが可能となります。
「私たちが開発したシンプルなセンサーで、表面化学の難問を解くことができます」と、nMISセンサーの開発に携わったバーラ・ニキル博士は言います。
同一の装置上で表面化学反応の基本的な2つの特性を測定することによって、マイクロ流体プラットフォーム内に生体分子が無事に封入できたことを確認することができます。もし電荷、もしくは質量のいずれかの1つだけの測定であれば、誤った解釈へ導く可能性があり、それは生体分子が実際は表面に定着していない場合でも、表面に生体分子が存在しているかのように見えてしまうことです。同一の装置内で2つ以上の技術を有していれば、同じ結果であるかどうかを別の測定に切り換えて調べることができます。
「1つの反応の成否を立証するためには、複数の実験的検証により観測結果の信頼性を裏付ける必要があります。1つのプラットフォームで2つのパラメーターを同時に測定できるセンサーの実現は、センサー技術の開発に携わる研究者にとって大きなメリットとなります」と、ニキル博士は期待をにじませます。
「2つの計測機能を併せ持った小型のプラットフォームは、持ち運び可能な高感度センサー技術の実現を可能にします」と語るのは、OISTで博士課程を履修しているシヴァニ・サティッシュさんです。
本研究における実証実験では、生体分子の質量と電荷の両方の情報を組み合わせることによって、一定のエネルギーレベル以下のイオン化ガスを暴露させた場合では、一般的な生体分子は残ることが示されました。電荷だけのひとつの情報だけからは誤った解釈が導かれる一方で、相補的な因子を組み合わせることにより、信頼性の高い生体分子の検出が可能となります。
この優れたnMISセンサーは、様々な疾患を分析するためのマイクロ流体プラットフォームの創出に役立つことが期待されます。nMISセンサーを使用して電荷と質量を測定することで、疾患を検出する生体分子が確実に封入され、診断装置の中で機能することを保証することができます。
「市販の妊娠検査薬のようなものです」と、同研究チームを率いるエイミー・シェン教授は言います。「使用前にあらかじめ必要な試薬が組み込まれていれば、あとは血液や尿といった検体を加えるだけでいいのです」。
さらなる可能性として、異なる標的に作用する複数のバイオマーカーを1つの検査装置に導入することが挙げられます。2種類の特性を測定することが可能なセンサー技術と、準備不要の検査装置を組み合わせれば、在宅や診療室でおこなわれるその場診断が可能となり、医療診断分野に大きな革新をもたらすことが期待されます。
報道関係のお問い合わせ