微小な液滴から生きた細胞内部の実像を垣間見る

本研究のポイント
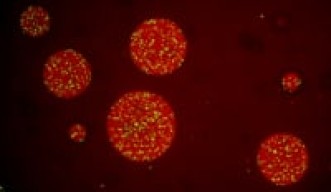
- 細胞内のタンパク質移動や相互作用を模倣した膜のない微小な液滴を作製した
- この液滴を使うことによって、システムの複雑さを損なうことなく、酵素反応を適切に制御して研究することができる
- 研究チームは、ポリエチレングリコール(PEG)と呼ばれるポリマーとタンパク質を水性緩衝液に混合させ、タンパク質を多く含む液滴を形成した
- これに酵素(化学反応を誘発したり制御したりするタンパク質)を加えると、細胞内で起こる反応を液滴で再現できることがわかった
- また、その化学反応は微生物と同じような速度で起こっていた。
本文
細胞の中では、物質が密集し、慌ただしく動いています。タンパク質などの分子は、細胞内を満たす液体である細胞質基質(サイトゾル)の中をかけ巡り、互いにぶつかり合っています。これらの分子間の相互作用が、細胞の活動の動力源となっています。しかし、これらの相互作用を科学的に研究する際には、非常に単純化されたシステムを使用するため、その複雑さを捉えることができませんでした。
この度、沖縄科学技術大学院大学(OIST)の研究チームは、分子の密度と動きが生きた細胞内と類似する、膜のない液滴を作製しました。本研究を主導したOISTタンパク質工学・進化ユニットのパオラ・ラウリーノ准教授は、Nature Communications誌に掲載された本手法により、分子が生きた細胞中でどのように振る舞うかをより忠実に反映した方法で、細胞の反応を研究することができるようになると述べています。
細胞中に存在する重要な分子のひとつに、酵素と呼ばれるタンパク質の一種があります。酵素には、化学反応を誘発し、その進行速度を調節する役割があります。酵素を研究するには、まず他の分子を含まない大量の水性緩衝液に酵素を加え、酵素が作用する「基質」と呼ばれる物質を加えます。そして、その反応過程を観察します。この際に使用する緩衝液は、非常に希釈されたものです。ラウリーノ准教授は、「酵素は精製されており、中に何が入っているかが完全にわかるので、良いシステムです。しかし私たちは、高分子が密集したサイトゾルに似たシステムを作製し、これが酵素の活性にどのような影響を与えるかを見てみたかったのです」と説明します。
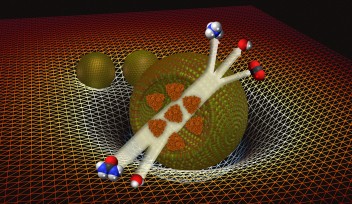
ラウリーノ准教授は、スイスのチューリッヒ工科大学やドイツのマックスプランク研究所の研究者を含む共同研究チームとともに、ポリエチレングリコール(PEG)と呼ばれるポリマーとタンパク質を水性緩衝液の中で混ぜ合わせて液滴を作製しました。PEGポリマーを混ぜることで緩衝液中の密度が高くなり、タンパク質を多く含む微小な液滴が緩衝液中で分離されます。次に、この混合液に酵素を加えると、酵素は液滴中に拡散していきます。液滴内は非常に濃度が高いため、反応チャンバーとなり、酵素が反応を起こします。研究チームは、液滴中の反応の速さと分子の物性を追跡しました。
研究チームは、混合液に乳酸脱水素酵素を加えると非常に効率的に反応が起こることを発見しました。これは、微生物において見られるような非常に高い代謝速度です。「このことは、液滴の中に大量のエネルギーを蓄えることができることを意味しています」と、ラウリーノ准教授の研究ユニットに所属するミルコ・ディンド博士は述べています。
次に研究チームは、反応中に水素イオン濃度を示すpHの変化を促すウレアーゼという別の酵素に変更しました。 これにより、液滴中にpH勾配が生じ、強い分子流が発生しました。「細胞内で起こるこの現象は原形質流動と呼ばれ、物質が混ざったり移動したりする上で非常に重要なメカニズムです。これを実験室で再現できるというのは、非常に興味深いことです」と、ディンド博士は述べています。
研究チームは緩衝液に加えたタンパク質と酵素の量を把握しているため、反応は適切に制御されています。ラウリーノ准教授は、この研究成果によって細胞内で起こる現象の「実像に一歩近づいた」とし、次のように述べています。「これで私たちは、サイトゾルの特性の一部を再現する制御可能なシステムを手に入れました。このシステムを使って、さまざまな酵素を系統的に研究し、タンパク質の密度や代謝速度などの特性が酵素活性にどのように影響するかを調査することができます。」

ライター: Alla Katsnelson
論文詳細
- 論文タイトル: Sustained enzymatic activity and flow in crowded protein droplets
- 発表先: Nature Communications
- 著者及び所属先:
- Department of Materials, ETH Zürich, 8093, Zürich, Switzerland- Andrea Testa, Aleksander A. Rebane, Robert W. Style & Eric R. Dufresne
- Protein Engineering and Evolution Unit, Okinawa Institute of Science and Technology Graduate University, 1919-1 Tancha, Onna, 904-0495, Okinawa, Japan - Mirco Dindo & Paola Laurino
- Max Planck Institute for Dynamics and Self-Organization (MPIDS), D-37077, Göttingen, Germany - Babak Nasouri & Ramin Golestanian
- Rudolf Peierls Centre for Theoretical Physics, University of Oxford, Oxford, OX1 3PU, United Kingdom - Ramin Golestanian
- DOI: 10.1038/s41467-021-26532-0
- 発表日: 2021.11.01