2017年5月30日
自己免疫疾患の発症につながる新たな分子メカニズムの発見
概要
この度、沖縄科学技術大学院大学(OIST)の研究チームは、自己免疫疾患の発症に深くかかわる分子メカニズムを発見しました。
研究チームは、これまで自己免疫疾患の発症に密接に関与することが明らかになっている「Th17細胞※1」(良性と悪性がある)をターゲットとする自己免疫疾患の治療法開発に向けた基礎研究を行う中で、「JunB」という転写因子※2タンパク質のひとつが、悪性のTh17細胞が固有の機能をもつように成熟する(分化する)際に必要であることを明らかにしました。一方、マウスを使った実験で、良性のTh17細胞の誘導には「JunB」が必要ないことも示唆しました。このことから、「JunB」は、有害なTh17細胞のみを狙い、且つ、良性のTh17に影響を与えることのない、副作用の少ない新たな自己免疫疾患の治療標的となる可能性があります。自己免疫疾患に関しては、現在、治療の中心となっているのは免疫システム全体を抑制するものですが、この治療法では患者の体が病気と戦う能力を低下させてしまうという問題があります。今回の研究成果は、こうした現状に新たな道をもたらすものと言えます。「JunB」のTh17細胞における機能が初めて明らかになった本研究成果は、英科学誌 Nature Communications に掲載されました。
研究の背景と経緯
私たちの身のまわりには、細菌やウィルス、花粉、粉塵など、生体に悪影響をおよぼす生物や物質が存在しますが、これら病原体の侵入から身体を守るのが免疫という自己防御機構です。ところが、免疫システムが正常に機能しなくなると、自己の生体成分や細胞を「異物」と認識して、特定の細胞や組織を攻撃してしまい、病気を発症します。これが自己免疫疾患※3です。このような望
ましくない免疫反応は、日本で約70〜80万人の患者数がいるという※4関節リウマチや、潰瘍性大腸炎、多発性硬化症といった自己免疫疾患を引き起こします。これらの疾患は先進国で特に増加傾向にあり、塩分過多および高脂肪を特徴とする欧米化した食生活がその一因であることも示唆されています。多くの自己免疫疾患は国が選定する指定難病となっており、その治療法の開発が重要な課題となっています。
近年、ヘルパーT細胞※5という免疫システムの司令塔の役割をしている細胞の一種「Th17細胞」が自己免疫疾患の発症に密接に関与することが明らかになってきています。これに伴い、Th17細胞の分化に必要な分子を標的とする自己免疫疾患の治療法の開発が世界中で行われています。自己免疫の原因となるTh17細胞は極めて強い炎症をおこす能力をもっています。しかし全てのTh17細胞がそのような高い炎症誘導能力をもつわけではありません。実際、私たちの腸には常に多数のTh17細胞が存在し、腸の正常な働きの維持にかかわることが示唆されています。したがってそのような良性のTh17細胞ではなく、自己免疫をおこす悪性のTh17細胞のみをピンポイントに狙う治療法が望ましいと考えられます。しかし、これまで、このような目的に適う分子メカニズムはほとんどわかっていませんでした。
そこでOIST免疫シグナルユニットの石川裕規准教授ら研究チームは悪性のTh17細胞の分化に特異的に関与する分子を見つけることを試みました。
研究内容
(1) 悪性Th17細胞の分化に関わる分子はどれか
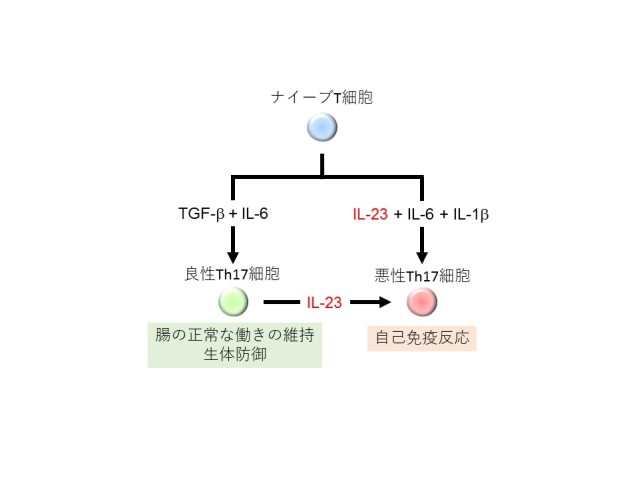
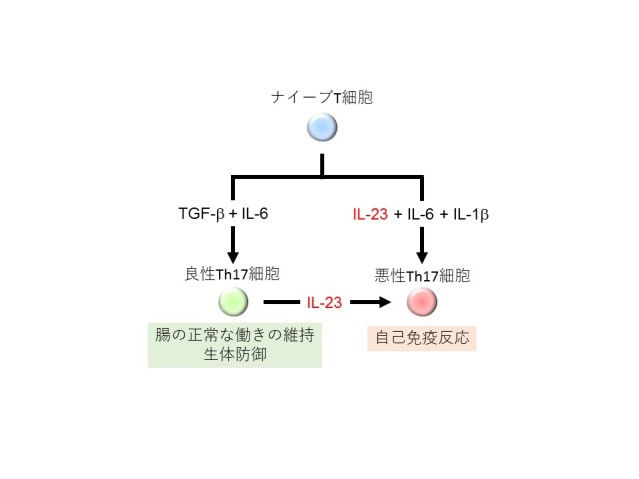
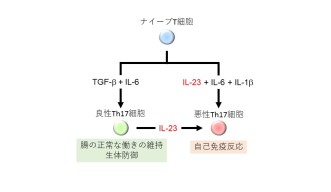
Th17細胞はナイーブT細胞※6が分化したものです。この分化は複数のサイトカイン※7(TGF-bやIL-23など)の刺激が組み合わさることで誘導されます。またサイトカインのタイプによってTh17細胞の悪性度が決定されることも知られています(図1)。
すなわちTGF-b存在下でつくられるTh17細胞は炎症を誘導する能力が低く、腸に常在する良性のTh17細胞に類似しています。一方、IL-23によってつくられる悪性Th17細胞は高い炎症誘導能をもち、自己免疫疾患を誘発します。また、IL-23は良性のTh17細胞を悪性Th17細胞へと変換することも知られています。しかしIL-23がどのような分子メカニズムで悪性Th17細胞の分化を促進するのかはよく分かっていませんでした。そこで本研究チームはIL-23による悪性Th17細胞の分化誘導にかかわる転写因子を探しました。具体的には、Th17細胞に発現する283個の転写因子のなかから、その発現を抑制した際に悪性Th17細胞の分化がおこらなくなるものを一つひとつ確認しながら探しました。その結果、転写因子JunBの発現を抑制した細胞では、悪性Th17細胞の分化が強く抑えられることが確認されました。
(2) 「JunB」の機能をマウスを用いて確認
JunBのTh17細胞分化における機能を明らかにするために、T細胞のJunB遺伝子を欠損したマウスを作製しました。まず、このマウスより分離したT細胞をもちいてTh17細胞の分化におけるJunBの重要性を検討しました。その結果、JunBはTGF-bによる良性Th17細胞の誘導にはあまり必要ありませんでした。一方、IL-23による悪性のTh17細胞の誘導に極めて重要であることが示されました。
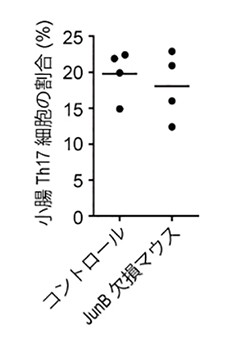
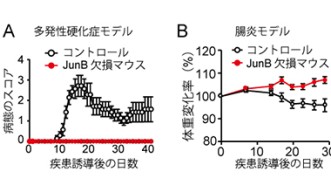
次に、JunB欠損マウスの小腸に局在するTh17細胞の数を調べました。その結果、JunBの欠損は小腸のTh17細胞数に影響を与えませんでした(図2)。これらの結果は、転写因子JunBが良性のTh17細胞の分化には必要ないことを示唆します。
(3) 「JunB」が悪性Th17細胞の分化だけに関わることを確認
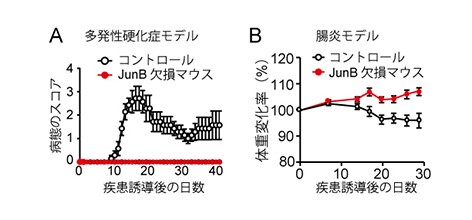
最後に、JunBの欠損が自己免疫疾患の発症に与える影響を評価しました。ここではヒトの多発性硬化症のマウスモデルおよびマウスの腸炎モデルのふたつを用いました。その結果、JunB欠損マウスは多発性硬化症をまったく発症しませんでした(図3A)。また、JunB欠損細胞は腸炎をおこしませんでした(図3B)。これらの結果は、JunBが自己免疫反応をおこす悪性Th17細胞の分化に特異的に必要であることを示しています。つまり、JunBが悪性Th17細胞のみを制御するための治療標的となることを示唆します。
今回の研究成果のインパクト・今後の展開
今回の研究成果は、良性のTh17細胞ではなく、自己免疫を引き起こす悪性のTh17細胞の分化において、JunBを介する転写メカニズムが必要不可欠であることを明らかにしました(図4)。研究を率いた石川裕規准教授は、「この新たな知見は、悪性Th17細胞をピンポイントに狙う副作用の少ない自己免疫疾患の治療法の開発のために重要です。」と、その成果を強調します。
また、本研究成果はTh17細胞の機能的多様性を生みだすメカニズムの一端を解明するものです。
Th17細胞は上述の機能に加えて、細菌や真菌に対する生体防御およびガンの排除にかかわることも知られています。石川准教授は、「Th17細胞の多様な機能とJunBの関わりは興味深い研究対象であり、その解明は有効なワクチンおよびガン免疫療法の開発につながる可能性があります。」と述べ、次なる研究について、「今後は、JunBによる転写制御メカニズムをより深く理解する必要があります。JunBを必要としない良性のTh17細胞の分化メカニズムを明らかにすることも重要な課題です。」と、意欲を示しました。このような研究は、合理的な免疫制御法の開発の基盤となり、より効果的で安全な自己免疫疾患の治療法の確立に貢献するはずです。
用語説明
※1 Th17細胞
サイトカインのひとつであるIL-17の発現を特徴とするヘルパーT細胞の一種。ヒトを含む哺乳動物の小腸には多数のTh17細胞が常在し、細菌や真菌の感染に対する防御および腸の正常な働きの維持にかかわることが示唆されている。一方で、Th17細胞には自己免疫疾患の原因となる悪性のものもあることが知られている。
※2 転写因子
特定の遺伝子群の発現を制御する因子であり、多種多様な細胞機能にかかわる。
※3 自己免疫疾患
自己の身体を構成する物質に対しておこる免疫反応により発生する疾患。関節リウマチ、多発性硬化症、炎症性腸疾患、全身性エリテマトーデスなどがある。それらの多くは特定疾患に指定される難病で、国内では年々増えている(難病情報センター特定疾患医療受給者証所持者数http://www.nanbyou.or.jp/entry/1356)。
※4 厚生科学審議会疾病対策部会リウマチ・アレルギー対策委員会 「リウマチ・アレルギー対策委員会報告書」平成23年8月より
※5 ヘルパーT細胞
成熟したT細胞(リンパ球)の一種。免疫反応を指揮する役割を果たす。
※6 ナイーブT細胞
未成熟なT細胞(リンパ球)であり、抗原と反応することでヘルパーT細胞などに分化する。
※7 サイトカイン
免疫細胞から主に分泌され、免疫細胞間の情報伝達に用いられる。各サイトカインはそれぞれ特有の機能をもつ。
- プレスリリース(PDF)