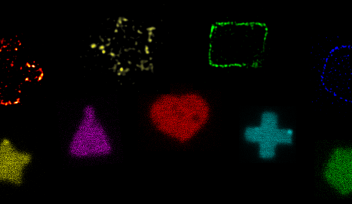2017年12月20日
バクテリアの細胞分裂に光を当てて
20分毎にその数が倍増する侵略部隊に立ち向わなくてはならない場面を想像してみてください。実際これは、人体が有害な大腸菌に感染したときに直面する事態です。急速に増殖する有害な大腸菌は宿主の人体に対し、下痢、呼吸器疾患、肺炎といった不快かつ危険な疾患を引き起こす可能性があります。
全世界的に抗生物質耐性菌の出現が増加している中、科学者らは薬物で細菌感染を阻止する新たな方法を懸命に模索しています。バクテリアの細胞分裂を阻止する有効な方法の一つは、細胞分裂及び増殖機構を標的にすることです。しかしそのためには、バクテリア細胞分裂機構の構造と仕組みをより詳細に把握しなくてはなりません。
この度、沖縄科学技術大学院大学の構造細胞生物学ユニットの研究者たちは、ストックホルム大学と共同で大腸菌の細胞分裂機構についての研究を行い、その成果をMolecular Microbiology誌に発表しました。
将来的に本研究は、抗生物質でバクテリアを標的にする新たな方法につながる可能性があります。「バクテリアの細胞分裂についてメカニズムの詳細を理解することができれば、それを阻害する薬の開発に取り組むことができるでしょう」と、論文筆頭著者のビル・セダーストゥル博士は述べます。
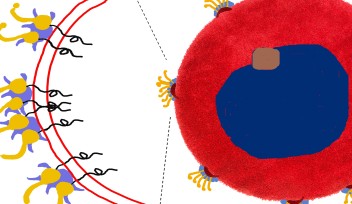
ほとんどのバクテリア細胞は、二分裂、すなわち母細胞にくびれが生じ、同じ2つの 娘 細胞に分離する、というプロセスを通して複製します。その細胞分裂の間、「divisome」と呼ばれる大きな分子機構が細胞内に形成されますが、この度セダーストゥル博士らは、大腸菌のdivisome主要構成因子である「 FtsZ」と「FtsN」という 二つの 重要なタンパク質の空間配置を明らかにしました。
これまで細胞生物学者の間では、divisome中のすべてのタンパク質は1つの 巨大複合体に集結していると考えられてきました。なぜなら従来の蛍光顕微鏡法では、分解能が比較的低く、非常に近距離で隣接している物体同士は単一の物体として見えていたからです。 しかし、この度 OIST研究者らは、 最先端の イメージング 技術である超分解能誘導放出抑制(STED)顕微鏡を使用することにより、 大腸菌の分裂機構をナノスケールで視覚化することに成功しました。「優れた分解能により、異なるタンパク質リングを差別化し、細胞分裂の過程における詳細を推論することができました」と、セダーストゥル博士は語っています。
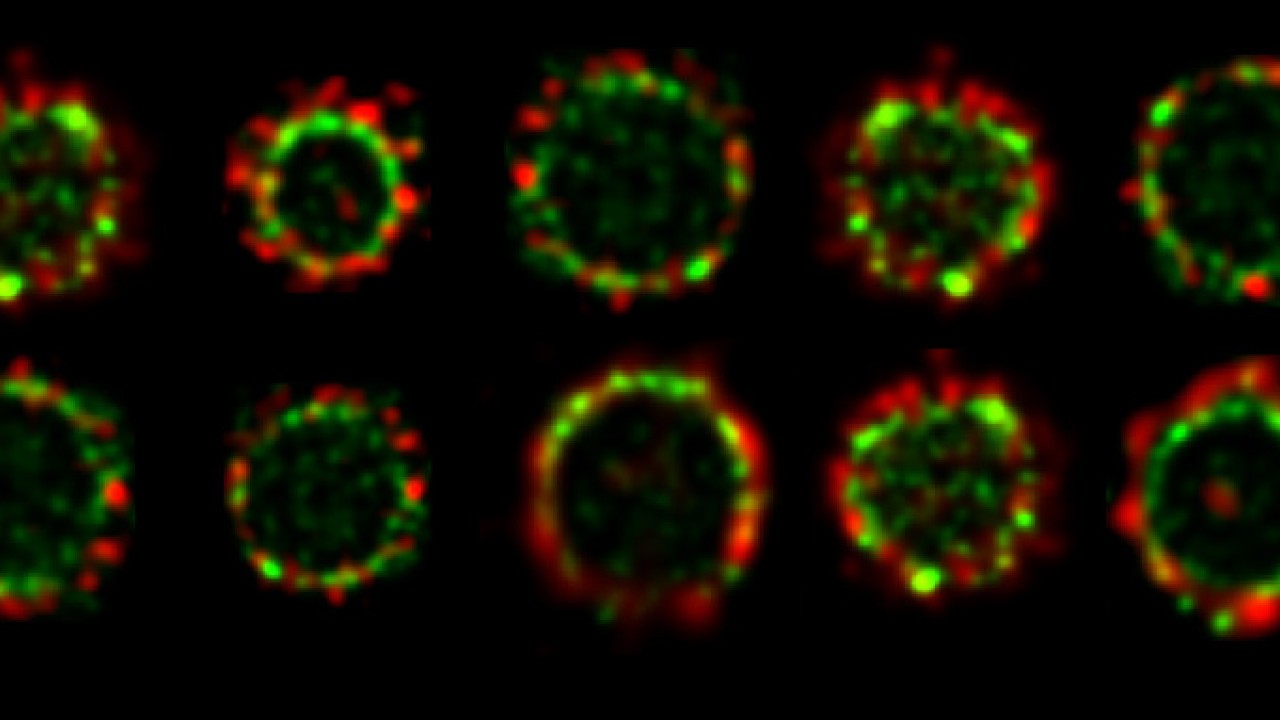
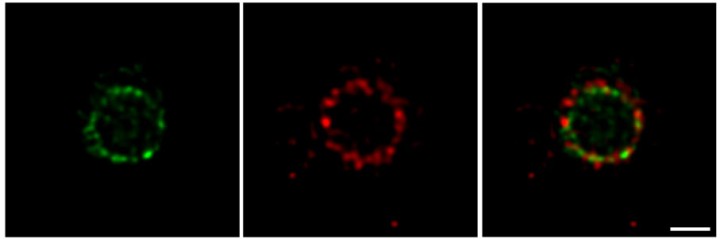
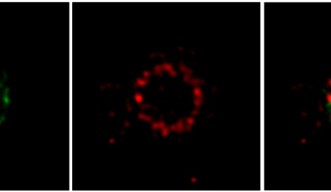
研究者らは、FtsZとFtsNに緑と赤の蛍光標識をそれぞれに付与することで、これらのタンパク質が大きな集合体として局在し、かつ細胞分裂部位の周辺に不均一に分布していることを 明らかにしました。細胞分裂初期においては、2つのタンパク質は重複しないパッチ状リング構造を形成します。細胞分裂が進行するにつれ、FtsZにより形成された緑色リングは、FtsNにより形成された赤色リングの内側に移動します。これらのタンパク質は常に重なっているのではなくいくつかのグループに分かれている、という知見により、divisomeは単一分子機構としては作用しておらず、むしろ各タンパク質グループがそれぞれ特定の役割を果たしていると考えられました。
細胞分裂機構のより詳細な全体像がわかれば、生物学者たちは、バクテリアの細胞分裂と増殖を 防ぐ新たな抗生物質を 設計することができます。「次のステップは、より多くの細胞分裂機構に関与するタンパク質を観察し、これらのうちどれを薬物で標的化すべきか、を 解明することです」と、セダーストゥル博士は意気込みを語っています。