2020年10月15日
異分野間の学際的アプローチで実施されたOIST抗体検査
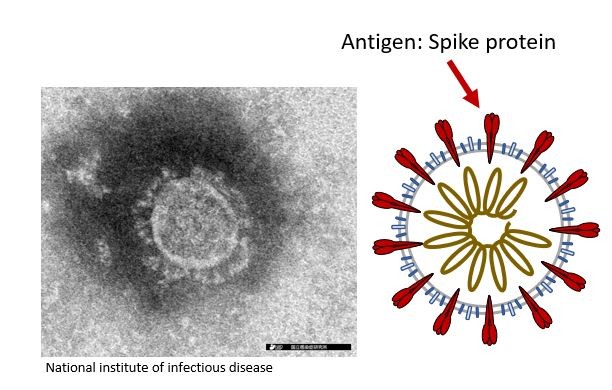
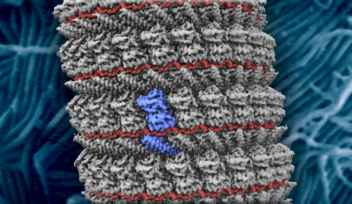
人がウイルスに感染すると、免疫システムが抗体を作り、体がウイルスと闘うのを助けます。免疫反応を引き起こす物質は抗原と呼ばれ、それを元に特異的に結合する抗体が作られます。新型コロナウイルスであるSARS-CoV-2の場合は、ウイルスの表面にあるスパイクタンパク質が主な抗原の一つです。抗体は体内のウイルスが消滅した後もしばらく血液中に残るため、酵素結合免疫吸着法、別名ELISA(Enzyme-Linked Immuno Sorbent Assay)と呼ばれる方法で抗体を検出することで、ウイルスの感染歴を知ることができます。
2段階プロセスで精度を確保
ニューヨークでSARS-CoV-2の初のELISA法が開発された3月初旬、マティアス・ウォルフ准教授は、プラスミドを沖縄に送ってもらいました。プラスミドにはスパイクタンパク質とその受容体結合ドメインをコードする遺伝子が含まれています。ウォルフ准教授は、以前にエボラウイルスの研究を行っており、SARS-CoV-2を検出するための研究を試みたいと考えていました。そして准教授の率いる生体分子電子顕微鏡解析ユニットは、OIST抗体検査に着手しました。
ELISAに必要な材料が到着すると、スタッフサイエンティストのキム・テギュン博士がスパイクタンパク質の発現と精製を始めました。検体に抗体が含まれるかどうかを確認するために必要な抗原たんぱく質を準備する作業です。
一方、研究者たちは、受け取った検体をより安全に検査するために、不活化する方法についても考えました。「私たちは検査を行う前に、検体をバイオセーフティレベル2の封じ込めシステムを備えた研究室内で、専用の遠心分離機を用いて血清を分離した後、加熱し不活化処理しました。」と、スタッフサイエンティストの柴田敏史博士は説明します。
すべての抗体検査が同じように作られているわけではありません。検査精度を最大にするため、OISTで使用されているアッセイは2段階のプロセスで構成されています。
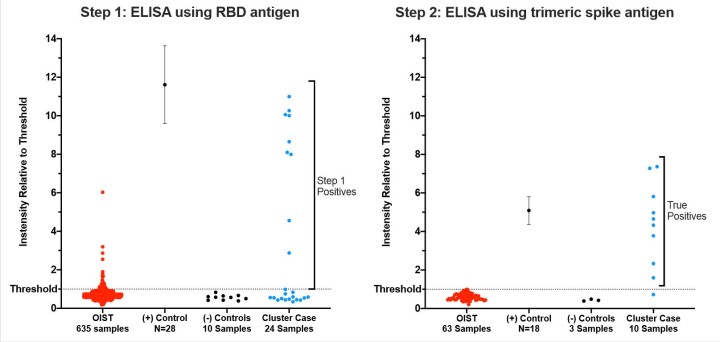
1段階目では、スパイクタンパク質の一部分を抗原として使用し、結合する抗体が検体中にあるかどうかを調べました。この検査は非常に感度が高いものの、ウイルスに特異的ではないため、低いレベルの抗体を感知することができますが、これは必ずしもSARS-CoV-2のものではありません。
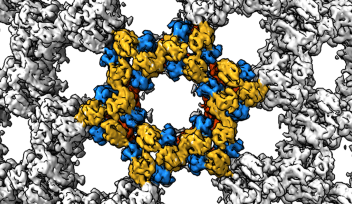
「血清がステップ1検査で疑陽性となった場合、ステップ2で再度検査します。ステップ2では、3量体スパイクタンパク質複合体抗原と段階希釈した血清を使用しました。このように検査することで検査精度が上がり、過去数ヶ月間にウイルスに感染した人からの検体のみが陽性となります。」と、同ユニットのポスドク研究員であるメリッサ・マシューズ博士は、説明します。博士は、研究助手の柴田則子さんとともに検査のセットアップを担当しました。
研究者たちは、OISTの外部から受け取ったコントロール試料を用いた対照実験により検査方法の精度を示しました。陽性対照試料として、4月のPCR検査でのSARS-CoV-2陽性者からの検体を使用しました。陰性対照試料は、SARS-CoV-2抗体を持たないことがわかっている昨年採取された血清を使用しました。いずれの場合も、これらの対照試料を各検査プレートに入れ、検査結果が正しいことを確かめました。
最後に、流体力学ユニットの技術者であるクリスチャン・ブッチャーさんが、検査の自動化に尽力し、検査容量を拡大することができました。この自動化がなければ、検査は手動で行われなければならず、効率が大幅に低下していたでしょう
OISTコミュニティの抗体検査
OISTの職員・学生を検査する際の問題点の1つは、どのように血液検体を集めるかで、医師がいなくても採血できる方法が必要でした。そこで、研究者たちは各自で指を穿刺し採血する方法を採用しました。自分たちでいくつかの既存の血液採取キットを試しましたが、キットは安全で、使いやすく、かつ安価なものでなければいけません。「結局、個々のパーツを注文して独自の血液採取キットを作ることになりました」と柴田博士は語ります。
血液採取キットの構成が決まった後は、実際にボランティアを匿名でどのように検査するかを考えました。IT部門の協力を得て、QRコードシステムを作成し、説明書や動画などのウェブサイトにリンクさせました。各キットには、検体管理バーコードとQRコードを付けました。バーコードは検体チューブに添付し、参加者は自身で保管したQRコードをスキャンして結果を得るしくみです。個人情報は保持されず、聞かれることもありません。
最後のハードルは、倫理的な承認を得ることでした。OIST人対象研究審査委員会の承認を得て、2020年8月に沖縄で第2波の流行時期に、OISTのコミュニティで検査を行う準備が整いました。
「私たちのチームは本当に一丸となっていました。タンパク質の発現、ELISA検査、ウェブサイトの作成、QRコード、バーコード、3Dプリンターによるチューブラックの作製、検査の自動化など、様々なことに取り組まなければなりませんでした。大学内の他のユニットの人たちにも手伝ってもらいました。私にとっても、ユニット全体にとっても、本当に活力を与えてもらった経験でした」と、ウォルフ准教授は振り返ります。
少数ですが、検査に十分な血清を抽出することが困難である検体もありました。これらの結果は、「未判定」としてウェブサイトから個別に知らされ、対象者は検査を繰り返すことができました。研究者たちは、OISTの職員・学生の協力によって提供された635の検体を調べました。その中でCOVID-19抗体が陽性となったサンプルはありませんでした。研究者らの結果は、medRxivのプレプリントサーバーに投稿された論文にまとめられています。また、県内医療関係者と協力して、診療所からの300のサンプルと那覇の小さなクラスターを検査しました。今後は、沖縄県庁との契約範囲内で提供される6,000検体を検査する予定です。