半世紀にわたるシナプスの探索

どうすれば研究を通じて社会に貢献することができるでしょうか? 沖縄科学技術大学院大学(OIST)細胞分子シナプス機能ユニットを率いてきた高橋智幸教授は、シンプルな答えを返します。「自分が一番好きな仕事に熱中して取り組み、得られた成果を多くの人々に発信することだと思います。」
同ユニットは高橋教授の引退に伴い、本日、2024年3月31日をもって閉鎖されます。
「私は常日頃、脳がどのような仕組みで働くのか、また、働かなくなるのかについて、不思議に思っていました」と高橋教授は話します。「医学部の学生時代に精神科の病院を見学する機会があり、現場の医師から治療の状況を伺ったところ、患者さんの3分の1は自然に回復し、3分の1は全く回復せず、残りの3分の1は治療薬が効いたかもしれないと感じられる、という説明でした。」
医師免許を取得後、臨床に進むか、基礎研究に進むかの分岐点にさしかかり、高橋教授は「自分の性格から、強い忍耐力が必要と思われる精神神経科の臨床は自分には向いていないと感じ、基礎医学研究を通じて、脳機能の仕組みを深く理解し、将来は脳疾患の治療に貢献したいと考えました。」
50余年後の現在、高橋教授は、新たな研究方法を開発して、数々の新事実を見出し、脳のはたらき全般を支えるシナプスの役割について、理解を深化させました。そして、脳疾患の救済につながる具体的な手掛かりを残しながら、今、引退の時を迎えました。

パッチクランプ解析からシナプスタンパク質解析へ
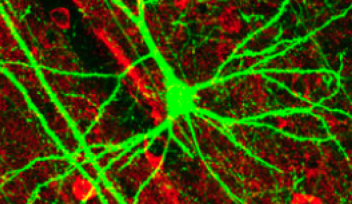
高橋教授の研究分野は神経科学であり、特に神経細胞間の接合部であるシナプスに焦点を置いています。シナプスは神経回路の情報の受け渡しに関わる重要な構造ですが、サイズが微小で、かつ脳組織の奥深く埋もれているために、直接的な実験解析が困難で、その機能メカニズムは謎に包まれていました。
70年代後半から80年代前半にかけてパッチクランプ法が開発される以前は、温血度動物の脳を単一ニューロンレベルで研究することは極めて困難であり、脳機能や脳機能不全を研究する上での大きなハードルとなっていました。パッチクランプ法は、細胞膜とガラス微小電極先端との間にタイトなシール(パッチ)を形成し、細胞膜内外の電位差を正確に測定し制御(クランプ)することを特徴としますが、電極先端の膜を陰圧をかけて破ることによって、単一細胞の電気的特性を非常に高い精度で測定することができます(ホールセル記録)。高橋教授は70年代後半にラットの脊髄切片上にニューロンを可視化して、微小電極により細胞内記録を行うことに既に成功していましたが、80年代後半、共同研究者と共に、脳切片上に可視化したニューロンにパッチクランプ法を適用して、安定で精度の高い記録が可能なスライス・パッチクランプ法へと発展させました。以来、この手法は、脳機能を細胞レベルで解析するためのゴールドスタンダードとなっています。

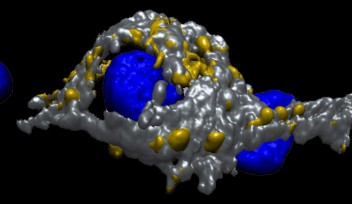
90年代に高橋教授はスライスパッチ法をヘルドの萼状シナプスに適用して、シナプス前末端の探索を始めました。このシナプスは脳幹の聴覚野にあって、音源定位情報を中継する巨大シナプスです。高橋教授はOIST内外の共同研究者と共に、この巨大シナプスをスライスおよび細胞培養標本に可視化して、神経伝達とシナプス可塑性の基礎研究を行いました。
高橋教授と共同研究者たちは、モデルシナプス標本を使って、シナプスタンパク質の機能的役割を同定し、さらに、アルツハイマー病、パーキンソン病などの神経変性疾患の標的タンパク質を明らかにしました。すなわち、シナプス前末端において、タウ、アルファシヌクレインなどの病因タンパク質の可溶性成分が微小管を過剰形成させることによってエンドサイトーシスが阻害されることが判明しました。これは微小管がエンドサイトーシスの重要な担い手であるダイナミンに結合して捕捉することによることが実証されました。シナプス前末端においては、エンドサイトーシスと小胞リサイクリングを経て伝達物質を充填した小胞が、放出部に確実に供給されることが神経伝達に維持には必要不可欠ですが、可溶性のタウやアルファシヌクレインによってエンドサイトーシスが阻害されると、神経伝達が維持できなくなり、記憶形成や運お動制御にかかわる脳領域の神経回路機能が破綻します。シナプス機能不全の分子メカニズムが見つかったことにより、機能的観点からアルツハイマー病やパーキンソン病の治療薬をデザインすることが可能になりました。「我々の研究はシナプス機能不全のメカニズムを明らかにして、これに基づく治療基盤を打ち立てたものですが、この土台に立って、様々な治療薬をデザインして投与し、モデル動物の行動に対する効果をテストすることによって、神経疾患からの救済をもたらす薬物が得られることを強く確信します」と高橋教授は話します。

分野の壁とテニスネットを越えて
質の高い研究をめざす一方で、高橋教授はテニスも熱心に練習してきました。テニスコートでは、心身の健康を維持するだけでなく、仕事の取組み方にもヒントが得られたと言います。「テニスでは、飛んでくるボールを返球する前に、どこに打つかを判断する時間の余裕を確保する必要があります。同様に、研究では、特定の疑問に明確な回答を与えるための実験を予めデザインする時間を確保する必要があります」と話します。
高橋教授は、どの研究分野に取り組む場合も、心底から興味の湧くシナプスに焦点を当ててきました。生物物理学、薬理学、分子生物学の分野の枠を越えて仕事を進めることは容易ではありませんでしたが、これによってシナプス機能の謎を探求することが可能になりました。若手研究者へのアドバイスを問われて、高橋教授は、「研究の初期段階で、自分にとって一番面白く、重要と思われる大きな疑問を見つけ、教科書や文献からでなく、自然から直接答えを引き出すことが大切です。自分の実験結果を十分に吟味、評価して、次の決め手を考える際に、答えを引き出すためには、既存の方法を越えて新しい実験方法を開発することが必要になるかもしれません。このように十分な準備をしておくことによって、大きな発見のチャンスが訪れることでしょう。」
細胞分子シナプス機能ユニットは2024年3月末をもって閉鎖されますが、タウ・タンパク質に関して発見した内容を論文としてまとめる、最後の仕上げを続けています。退職後、高橋教授はOIST赴任前に在籍した京田辺の同志社大学のキャンパスに近い自宅に戻って、脳科学研究科や生命医科学部の研究者達と交流を続けたいと考えています。

広報・取材に関するお問い合わせ
報道関係者専用問い合わせフォーム