パーキンソン病の新たなメカニズムが明らかに

沖縄科学技術大学院大学(OIST)の研究員らは、パーキンソン病関連タンパク質αシヌクレインが神経細胞(ニューロン)に過剰に発現することによって生じる毒性のメカニズムを同定しました。このタンパク質はパーキンソン病の発症に関わる原因物質として知られています。
本研究により、パーキンソン病発症の仕組みを探る上で、早期治療法の開発につながる重要な基礎知見を得ました。
本研究成果は、北米神経科学学会が発行する「ジャーナル・オブ・ニューロサイエンス The Journal of Neuroscience」のオンライン版に掲載されました。
研究の背景と経緯
パーキンソン病は世界中で約一千万人の人々が罹患している神経疾患で、日本人の1000人に1~1.5人(60歳以上では100人に1人)が発症している※1と言われています。この病気は進行性の運動機能障害と、典型的症状としての制御不能な震えを特徴とし、中枢神経細胞の機能障害、次いで神経変性、細胞死をもたらすものです。この病気に根治療法はなく、研究者は長年、病因の解明に取り組んできましたが、1990年代に、この研究分野に飛躍的進歩があり、タンパク質αシヌクレインの過剰がパーキンソン病の発症に関わることが明らかになりました。αシヌクレインは通常、主として脳に発現しており、特に神経細胞の軸索終末端に局在する機能不明のタンパク質です。
研究内容
OIST細胞分子シナプス機能ユニット(高橋智幸教授)の江口工学研究員(現:Institute of Science and Technology Austria)らは、ニューロンで過剰発現したαシヌクレインの毒性の第一標的が、神経終末端の小胞回収エンドサイトーシス機構であることを突き止めました。エンドサイトーシスは脳の高次機能を支える神経伝達に関わる主要ステップです。
1. αシヌクレイン過剰によって神経伝達の持続維持が損なわれることを発見
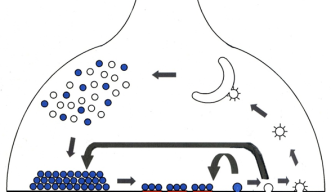
神経伝達は神経細胞間の接点、シナプス、で運動、知覚、認知などに必要な信号を受け渡すプロセスです。活動電位の信号が神経末端に到達して、次のニューロンに受け渡される際に、小胞※2内に充填されている伝達物質がこのプロセスを媒介します。小胞は脂質膜の袋で、伝達物質は小胞内からシナプス間隙(ニューロン間の隙間)に放出され、空になった小胞は、神経末端内に回収されて、再利用されます。一方、シナプス間隙に放出された伝達物質は次のニューロンの受容体と結合することによって信号を受け渡します (図1) 。
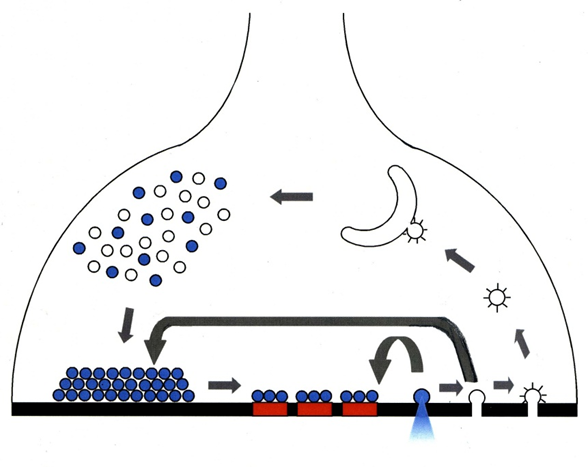
小胞膜の回収は「エンドサイトーシス」※3と呼ばれ、このプロセスが過剰のαシヌクレインによって障害を受けます。
「神経末端のエンドサイトーシスが抑制されると、小胞リサイクリングが失速し、小胞の供給が不充分になります」と高橋智幸教授は説明します。「小胞を適度に使っているときは問題ありませんが、大量に使われる場合に問題が生じます」。
高頻度神経伝達は、知覚認知、記憶形成、運動制御にとって重要ですが、このような場合に小胞が大量に使われます。研究チームは、αシヌクレインによってエンドサイトーシスが抑制されると、高頻度神経伝達が正常時のように維持できなくなることを見出しました。
2. 過剰αシヌクレインの毒性メカニズム
過剰αシヌクレインがエンドサイトーシスを抑制するメカニズムを更に研究したところ、微小管の過剰形成が関わることが明らかになりました。
「微小管は細胞骨格タンパク質で、言わば家屋の柱のようなものです」と高橋教授は説明します。「どうやら過剰のαシヌクレインが微小管の過剰形成をもたらして、エンドサイトーシスを阻害するようなのです。柱が不必要に多い家が住みづらく、室内の移動もままならないことは容易に想像されます。」
OISTの研究者たちは、過剰のαシヌクレインによる、この抑制過程がパーキンソン病の初期、未だ神経変性などの形態的変化が起こっていない時期に起こると考えています。
今回の研究成果のインパクト・今後の展開
今回の研究成果がパーキンソン病の治療法の開発に役立つかどうかという問いに対して、高橋教授は、「シヌクレインの第一標的が分かり、そのメカニズムも分かって、目標に近づいています。しかし、研究成果を治療法の開発につなげるためには、過剰の微小管がエンドサイトーシスを妨げる仕組みの詳細を更に明らかにする必要があります」と答えています。
※1パーキンソン病発症率
難病情報センター(http://www.nanbyou.or.jp/entry/169)
※2 シナプス小胞
軸索末端内に散在する球形の袋。伝達物質を充填しており、軸索末端膜と融合して、伝達物質を末端外に放出する。次いで、軸索末端膜が陥入、切離して小胞を再形成し、伝達物質を充填して、放出部位に輸送供給される。これによって神経伝達が維持される。
※3 エンドサイトーシス
軸索末端の膜が内側に陥入して、切離することによって小胞が再生される(図1参照)。この過程はエンドサイトーシスと呼ばれる。

プレスリリース(PDF)
研究ユニット
広報・取材に関するお問い合わせ
報道関係者専用問い合わせフォーム